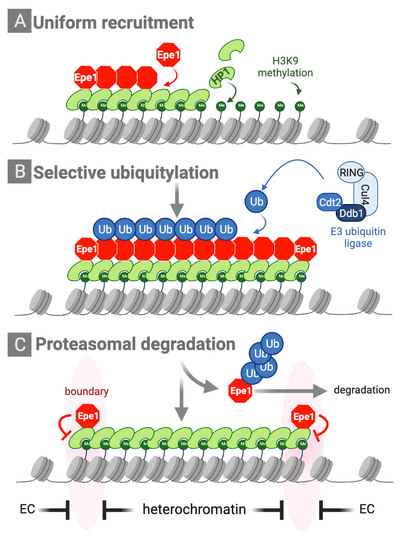
Abgrenzung und Aufrechterhaltung von Heterochromatindomänen
Die Unterteilung in aktives und stilles Chromatin erfordert spezielle Mechanismen zur Abgrenzung und Aufrechterhaltung der Identität von Chromatindomänen. Wir haben einen neuen Mechanismus entdeckt, der die Chromatin-Assoziation eines Anti-Silencing-Faktors und dessen Verteilung innerhalb von Heterochromatin durch Ubiquitin-abhängigen Proteinabbau reguliert. Dieser Mechanismus, den wir als "Chromatin-Sculpting" bezeichnen, ist essentiell für die Abgrenzung und Aufrechterhaltung von Heterochromatin-Abschnitten (Braun et al., Cell 2011). Die Integrität von Chromatindomänen kann auch dadurch aufrechterhalten werden, indem Faktoren und Histon-modifizierende Enzyme an spezifische Chromatinbereiche verankert werden; hierdurch wird die promiske Bindung an andere Genomabschnitte verhindert. In Zusammenarbeit mit der Arbeitsgruppe von Marc Bühler konnten wir zeigen, dass die Histon-Acetyltransferase Mst2 über ihr Partnerprotein Pdp3 an euchromatische Bereiche verankert wird. Diese Bereiche sind transkriptionell aktiv und mit methylierten H3K36 markiert, welches von Pdp3 erkannt wird. Dieser Verankerungsmechanismus verhindert, dass Mst2 von Euchromatin dissoziiert und in Heterochromatinbereiche eindringt und dort einen Silencing-Defekt auslöst (Flury et al., Mol Cell 2017; Georgescu et al., Microbial Cell 2020).